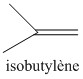La chimie du ballon de basketball (première partie)

Étant un grand fan de basketball, je ne peux m'empêcher d'écrire mon premier article sur la chimie du ballon de basketball. Et que de choses à dire sur cet équipement indispensable ! Les exigences des fédérations sont très strictes et précises sur la qualité du ballon, ainsi donc le choix des matériaux et des procédés de fabrications sont réfléchis en conséquence. Voici donc pour commencer un rapide résumé des règles de la WNBA à propos du ballon de basket :
- Parfaitement sphérique, circonférence correcte
- Etre résistant à l’usure
- Valve et ballon étanches
- Rebondir correctement
- Balle pas trop lourde (environ 600 g)
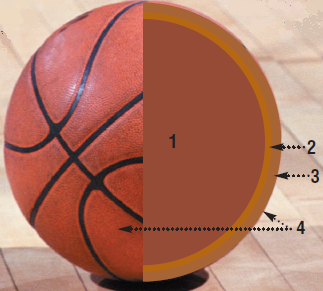
La composition d’un ballon de basketball
1. La poche intérieure
La poche sphérique intérieure se doit d’être complétement imperméable aux gaz, notamment ceux présents dans l’air (O2, N2) pour que le ballon reste correctement gonflé. Mais cette poche doit aussi être élastique et assez résistante.
Le simple caoutchouc s’il répond aux deux exigences précédentes, n’est cependant pas assez hermétique aux gaz. Ainsi c’est un matériau proche de ce dernier qui est employé : le butyle caoutchouc. Ce polymère élastique est très célèbre pour son excellente imperméabilité aux gaz, il est notamment utilisé dans l’industrie les pneus, les chambres à air, les joints industriels.
Avant d’expliquer la structure du butyle caoutchouc, il est important de comprendre ce qu’est un polymère. Un polymère est constitué de macromolécules. Ces dernières sont des molécules de masse molaire très grandes, et caractérisées par la répétition de petites molécules : les monomères.
Exemples de polymères naturels :
- Le caoutchouc
- Les protéines (polymères d’acides aminés)
- ADN
- Amidon
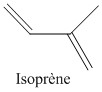
Le caoutchouc butyle est lui un copolymère de l’isobutylène et de l’isoprène, cela signifie que sa structure est constituée par la répétition de ces deux monomères. Le caoutchouc butyle est en fait surtout constitué d'isobutylène et contient peu d'isoprène ( environ 2% pour une chaîne).
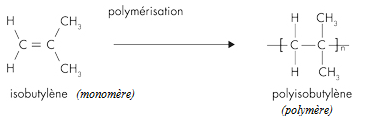
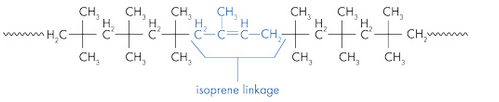
Initialement le matériau ne contenait que l'isobutylène, on obtenait alors le polyisobutylène (PIB), puis afin de lui donner des propriétés élastiques (caoutchouc), on a ajouté une petite quantité d'isoprène. Ce dernier va permettre d'introduire dans le polymère des doubles liaisons C=C.
www.techniques-ingénieur.fr
Structure du caoutchouc butyle :
www.techniques-ingénieur.fr
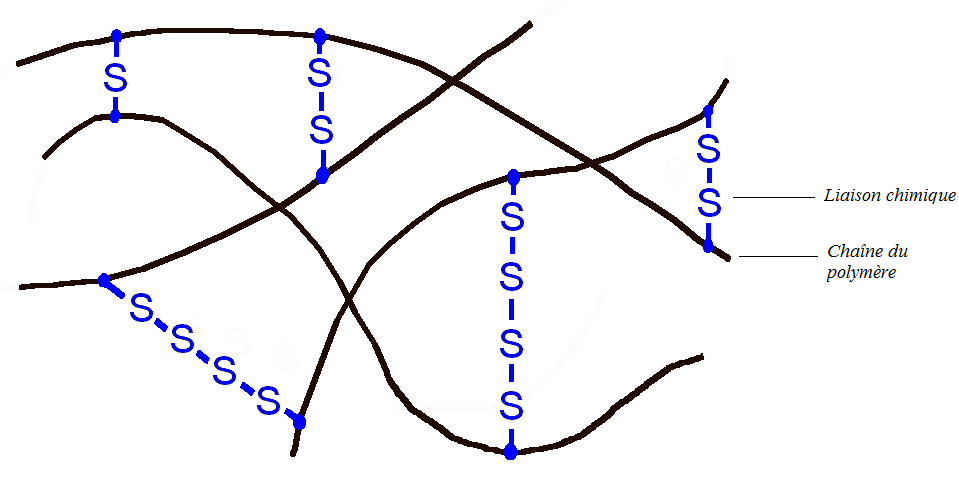
La présence de la double liaison C=C est très importante, en effet on a introduit dans le polymère un groupe fonctionnel réactif. L'objectif est alors de relier chaque chaîne de polymère par des liaisons chimiques, ce qui est possible grâce aux doubles liaisons. Ce processus se fait à haute température et en présence de soufre (agent vulcanisant) : c'est la vulcanisation.
Vulcanisation du butyle caoutchouc
Wikipédia
Le matériau devient alors beaucoup plus élastique, c'est un élastomère. Ce dernier peut alors être étiré jusqu'à deux fois sa taille originale et revenir très rapidement à sa forme initiale : voilà l'origine du rebond de la balle de basket. Une autre caractéristique intéressante est que le matériau n'est constitué que d'une seule molécule géante. Ainsi les différentes parties de la molécules ne peuvent plus se déplacer les unes par rapport aux autres quelque soit la température. Le matériau ne peut alors plus être fondu (état liquide). Ainsi si l'on brûle un ballon de basket, petit à petit ce dernier va se carboniser sans passer par un état liquide. (NB : les fumées noires provenant de la combustion sont toxiques et cancérigènes).
Ce dernier point démontre qu'il est important de bien donner la forme sphérique à notre caoutchouc butyle juste avant la vulcanisation du matériau, car il est ensuite impossible de fondre notre matériau pour lui donner la forme désirée.
Première couche du ballon de basket composée de caoutchouc butyle
alibaba.com
Exemple de gants fait en caoutchouc butyle

protective.ansell.com
vidéo où l'on brûle un ballon de basket
Attention ! Risques importants liés à une telle expérience : manipulation du feu, risques d'incendie, de brûlures importantes, toxicité des fumées...
La deuxième partie de cet article sera traitée la semaine prochaine avec au programme : les couches 2,3,4 ainsi que la synthèse et les propriétés du nylon. Bonne semaine :)
Références
- article ChemMatter, février 1999, "The chemistry of basketball"
- www.techniques-ingenieur.fr
Autres articles